飛行時間形質量分析計の原理と応用
概要
原子・分子の重さを調べるには体重計のようなハカリは使えず、質量分析 計では電場、磁場などの中でのイオンの運動を利用する。得られるデータはマススペクトルであり、目的成分の質量情報や含有量情報を読み取ることができる。 本稿では、近年のライフサイエンスの発展に大きく貢献した質量分析計のうち、飛行時間形質量分析計(time of flight mass spectrometer: TOF-MS)について述べる。飛行時間形質量分析計は、特に分子量が数十万に及ぶタンパク質など生体物質の同定、定性に利用されたことから生化学の分野 で広まり、今日では合成ポリマーなどの高分子や、医薬品、代謝物などの低分子の精密測定にも用いられている。
1. はじめに
質 量分析計はイオン化部、質量分離部、検出部に分かれ、質量分離部でイオンはm/z によって分離されるが、イオンの質量分離には種々の機構がある。TOF-MS は、イオンの速度を利用するが、装置の基本構成は高真空容器内のイオン加速のための電極と検出器のみといえる(図1)。イオン化部において生じた試料分子 のイオンは、グリッド電極と対向する電極の間に印加した電位差により加速され、フライトチューブ内に導入される。同時に加速された複数のイオンは無電場領 域のフライトチューブを、質量に応じた一定の速度で直線状に飛行し検出器に到達する。この一定距離のイオンの飛行時間からイオンの質量を算出する。質量分 析では電気的に中性な分子を測定できないので、目的成分を気相中にイオンの形で取り出す必要がある。TOF-MS は原理上、一連のイオン群が検出器に到達した後に次のイオン化を行うため、レーザーイオン化のようにパルス状にイオン導入する手法が適している。
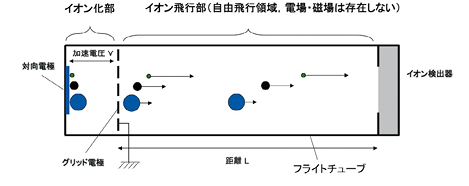
図1 飛行時間形質量分析計の模式図
2.原理
TOF-MS ではイオン化部で生成したイオンは、一定の電圧V によって加速される。イオンには式1に示す電圧に応じた運動エネルギーE が与えられ、フライトチューブ内を速度v で等速飛行する(q: イオンの電気量、V:加速電圧、m:イオンの質量、v: イオンの速度)。
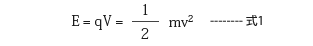
単位:m(kg)、q(C)、V(volt)
飛行距離をL とし、q=ze(z: 電荷数、e: 電気素量)を代入すると、フライトチューブを横切り検出器に到達するイオンの飛行時間t は式2 によって示される。
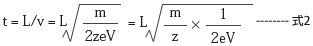
単位:t(秒)、L(m)
式2において距離L、加速電圧V、電気素量eはそれぞれ定数となるため、飛行時間t はm/z のルートに比例することが分かる。一定飛行距離では質量が小さいイオンは早く、質量の大きいイオンは遅く検出器に到達することになり、この時間差は質量差に変換できる。
式2において各項目の単位を、t(μ秒)、L(cm)、m(u またはDa)、z(イオンの価数)、V(volt)とすると以下の式が得られる。
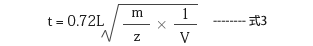
こ こでV=10 kV、L=100 cm とした場合、分子量約150 kDa のタンパク質であるIgG の飛行時間は 0.3 ミリ秒以下と算出される。TOF-MSはイオンの到着時間を測るだけであり、データ取り込みの間隔を延ばせば延ばしただけ、高質量のイオンの測定に対応で きるという特徴がある。
TOF-MS にはリニアTOF と分解能を向上させたリフレクターTOF があり、図2のように切り替えによって両モードが使える装置もある。レーザー照射から加速電圧印加の間に若干の時間差を持たせる遅延引き出し法の採用とあ わせ、分解能20,000 を超える装置も市販されている。
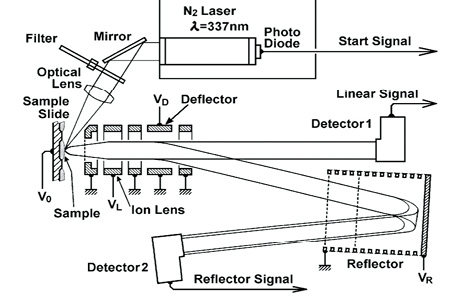
図2 市販のMALDI-T0F-MS の構成図
TOF-MS では理論上は、飛行時間を正確に測定することにより質量を算出できるが、実際は質量既知の標準試料を測定することにより質量校正を行う。質量校正用の標準 試料には合成ペプチドなどの混合物やNa-TFA などクラスターイオンが用いられる。近年ではフライトチューブの温調により外部の温度変化が原因の飛行時間のバラツキを抑えるなど、飛行時間の精度を高め る機構を組み入れることにより、外部標準法でも5ppm程度の質量誤差で測定できるようになった。
3.応用
TOF-MS は広い適用分子量範囲を持ち、また各種イオン化法と組み合わせることで広範な 化合物の分析に用いられる。TOF-MS は特にMALDI と接続することで微量のタンパク質やペプチドの分析に汎用的に用いられている。シナピン酸などのマトリックスと試料を試料ホルダに塗布・乾燥させ微細な結 晶に調製したのち、イオン化部に設置し、レーザー光を当てる。エネルギーはマトリックスを介して対象成分に移り、これらをイオン化させる。MALDI は溶媒に可溶で不揮発性であれば様々な生体関連物質、高分子をイオン化でき、分離精製無しで混合試料の直接分析が可能なことから、未知試料を予備的に分析 するのにも役に立つ。
a)TOF-MS による高分子の分析
図3にMALDI-TOF-MS による免疫グロブリンG(IgG)の測定結果を示す。IgG は分子量約150 kDa のタンパク質であるがpmol オーダーの試料量で分子量測定が可能である。図3ではイオン化の際に生じたと考えられる多量体のイオンが確認されるが、分子量58 万Da のイオンが測定できている。またタンパク質の酵素消化ペプチドのMS/MS スペクトルを測定し、データベース検索することによりタンパク質の同定を行うことも、プロテオーム解析での有効な手段である。このほかタンパク質の翻訳後 修飾の解析や、各種誘導体化法と組み合わせタンパク質の量的変動の網羅的解析が行われている。
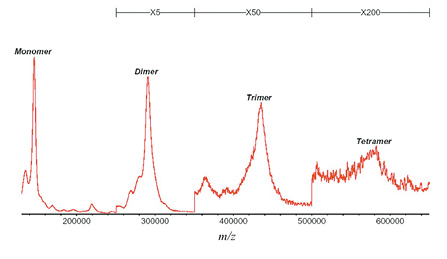
図3 MALDI-TOF-MS による免疫グロブリンG(150kDa)のマススペクトル
図 4にMALDI-TOF-MS によるポリスチレン製品の測定結果を示す。GPC と違い、MALDI-TOF-MS ではポリマー混合物中の個々の成分についての値が得られので、ポリマーを特徴づける様々な情報を得ることができる。これらのマススペクトルより、イオン化 されたポリマーの、モノ マー単位の質量を算出することや、末端基同定のための情報を得る、得られたポリマー分布から分子量関連データを計算する、などが行える。図4では、各イオ ンの質量差は104.1 と同間隔でありスチレン鎖の存在を示唆するが、試料によって分子量分布が2,500 を中心とするもの、7,000 を中心とするもの、13,000 を中心とするものなど、重合度の違いが区別できている。
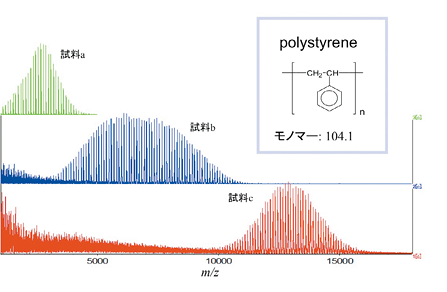
図4 MALDI-TOF-MS による合成樹脂の分子量分布確認
b)精密質量測定による組成推定
TOF-MS はその高い分解能、高い質量精度より、新規合成化合物や未知の天然物などの精密質量測定結果から組成式の推定が可能であり、構造解析に利用されている。図 5にLC-IT-TOF-MSを用いた市販の葛根湯のメタノール抽出液の正負極性切替LC/MS 結果を示す。TOF-MS をLCの検出器とする場合は、ESI のような連続イオン化と接続することになり、信号をパルス状に変換する機構が必要になる。LC-IT-TOF-MS ではイオン輸送部とイオントラップを連動させ、イオンをパルス状にフライトチューブに送り込むことでTOF-MS 測定を行っている。有効成分の一つであるグリチルリチンが9.7 分に溶出し、負イオンモードでm/z 821.3971 に脱プロトン分子と同定されるイオンを検出した。組成式から算出した脱プロトン分子の理論値と比較し、質量誤差5ppm以内の測定結果が得られており、組成式推定に適用できる精度が得られている。
【おわりに】
近年TOF-MS はMALDI によるオフライン測定のみならず、液体クロマトグラフのオンライン検出器としても用いられるようになっており、LC の汎用性にTOF の定性能力、高感度を付与した装置として利用できるようになった。今後もさまざまな分野で応用が期待される
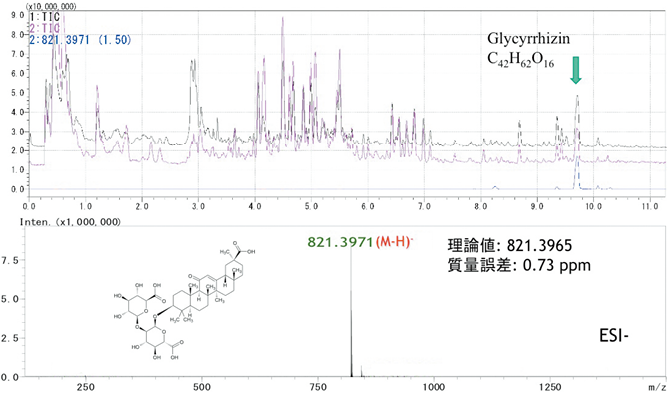
図5 LC-IT-TOF-MS による生薬成分の精密質量測定
八巻 聡
(株式会社島津製作所)
2016年5月2日 公開












