レーザラマン分光装置の原理と応用
1. はじめに
有機・無機材料の化学構造あるいは分子構造の分析手法として、ラマン分光法は近年さまざまな分野に応用されている。その適用範囲は電池、ディスプレイ、電子デバイス、食品/ 医薬品、バイオ分野など幅広く、カーボン、半導体、高分子、医薬材料などの成分分析や、結晶性/ 応力評価に威力を発揮する。最近では、生体組織や細胞の研究においても盛んに利用されている[1]。
2. ラマン分光法の原理
ラマン分光スペクトルは、化学構造あるいは分子構造を特徴づける指紋として捉えることができる。
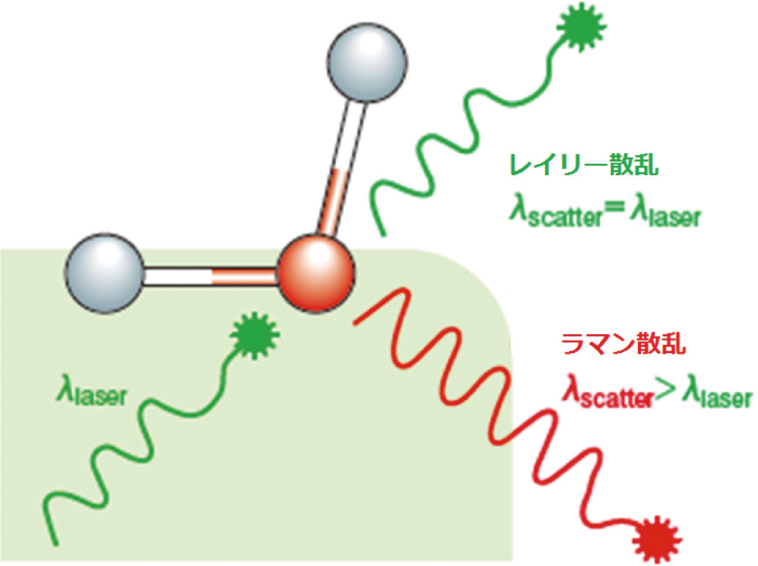
図1 ラマン散乱の原理
図1 に示すように、物質に光を照射すると散乱光が発生する。そのほとんどは照射光と同じ波長のレイリー散乱光であるが、わずかに波長の異なる散乱光も含まれている。これをラマン散乱光と呼ぶ。
レイリー散乱光とラマン散乱光のエネルギー差は、物質内の原子間振動のエネルギーに対応している。そのため、散乱光を分光したスペクトルには化学結合情報が反映される。ラマンスペクトルの横軸には、エネルギーに比例する単位として波数(波長の逆数)[cm-1] を用いるのが一般的で、レイリー散乱光の波数をゼロとした波数差(ラマンシフト)で表す(図2参照)。
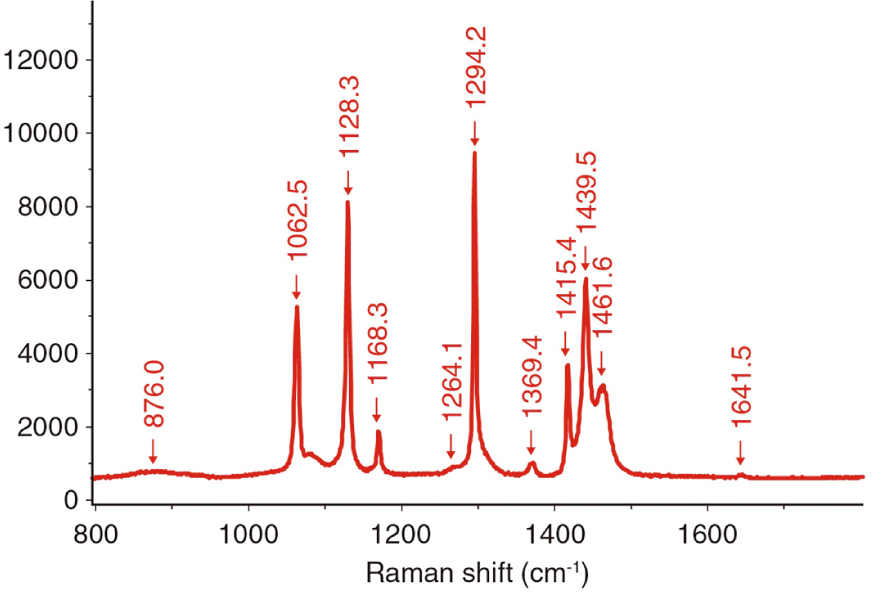
図2 ポリエチレンのラマンスペクトル
3. ラマン分光装置の構成
ラマン分光装置は、入射光源(レーザ)と分光器、検出器で構成され、ラマン散乱光のスペクトル測定に用いられる。最近では、顕微鏡と組み合わせた顕微ラマン分光装置がよく使われるようになってきた。
図3に堀場製作所製共焦点顕微ラマン分光装置LabRAM HR Evolution の構成を示す。本装置では、光源であるレーザ光を光学顕微鏡用対物レンズによりステージ上の試料に照射する。試料から発生したラマン散乱光を同対物レンズにて集光し、レイリー光カットフィルタを通して分光器に導く。
分光器の回折格子(グレーティング)により分散した光はマルチチャンネル検出器(CCD)を使ってスペクトルとして測定される。
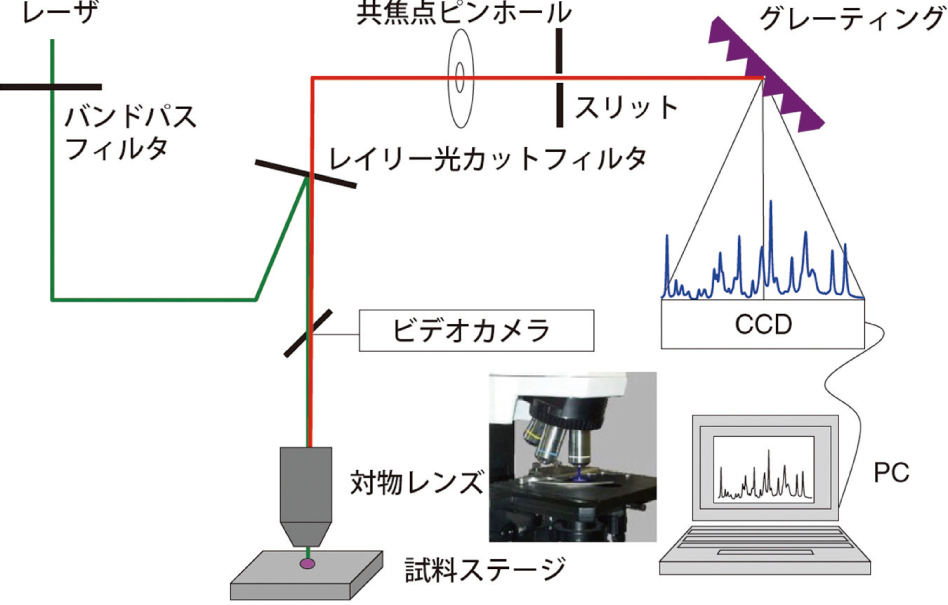
図3 共焦点顕微ラマン分光装置の構成図
4.特徴(長所・短所)
ラマン分光法の特徴は、固体のみならず、液体、気体のいずれの状態においても、大気雰囲気で特に前処理を必要としないで測定できることである。 可視レーザ光を分析プローブとして利用する場合、顕微ラマン分光装置では、約1 マイクロメータの空間分解能が得られ、マッピング測定によってラマンイメージを簡単に取得することができる。一方、短所として、ラマン散乱強度がレイリー散乱の百万分の一程度と非常に微弱であることがあげられる。このため、ラマン分光は感度が低い、あるいは競合現象である蛍光発生の影響を受ける、といった問題点が指摘されてきた。しかし、近年では、レーザをはじめとする光学部品の進歩と共焦点型顕微光学系の採用により、微小領域の測定でも短時間で良好なスペクトルが得られるようになり、試料から発生する蛍光の影響も軽減されている。
5-1. 応用例:電極材料の評価
リチウムイオン電池(LIB:Lithium ionbattery)の正極材料に使われるコバルト酸リチ ウム(LiCoO2)は,電池の劣化にともない酸化コバルト(Co3O4)に変化する。充放電サイクルテスト後に正極をLIB から取り出し洗浄した試料表面の測定結果から、図4に示すLiCoO2、劣化したLiCoO2(★はCo3O4 のラマンバンド)、カーボンのラマンスペクトルが観測された[2]。
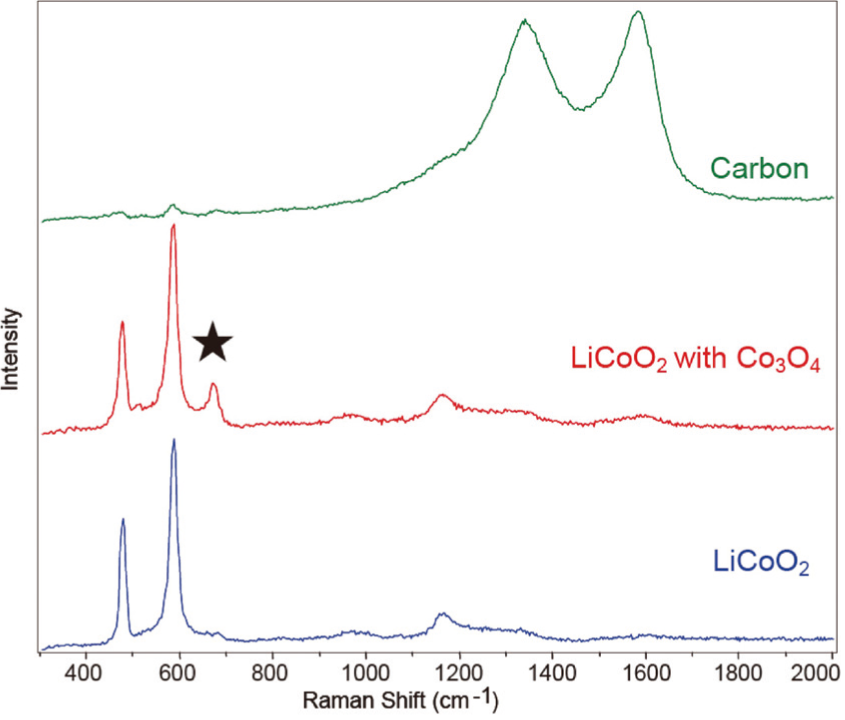
図4 LIB 正極のラマンスペクトル
ラマン分光法は、大気中/ 非接触で特に試料調製を必要としないため、石英製光学窓を持つ密閉セルにアルゴンガス中で密封したLIB を直接測定することができる。セル中のLIB を充放電サイクル試験にかけ、電極表面変化をラマンスペクトルの変化として捉えることができる[2]。
5-2. 応用例:半導体の応力評価
半導体デバイスなどに用いられる単結晶シリコンの応力評価にラマン分光が使われている。結晶に作用する応力により、シリコンのフォノンバンドがシフトすることが知られており、[110] 方向の一軸に対する [100] 面の応力 σxx [MPa] とピークシフト Δν [cm-1] の関係式は以下で表される[3]。
σxx = - 470.95 Δν[100]
5-3. 応用例:医薬品錠剤のラマンイメージング
医薬品錠剤中の複数の化学成分について,それぞれ異なる互いに重ならないラマンバンドの強度を使って、各成分の分布イメージを得ることができる。医薬品の活性成分にはいくつかの異なる結晶形(結晶多形)を持つものがあり、ラマンスペクトルを使ってこの違いも識別することができる[4]。
マッピング測定の高速化のために1 ピクセル当たりのスペクトル採取時間はミリ秒オーダーになってきている。採取時間の短縮に伴いスペクトルのノイズが増えるため、測定されたスペクトルからラマンバンドを特定する事が困難になる。そこで、多変量解析によるスペクトル分離手法がよく用いられるようになってきた。データ処理には、試料走査方向に対応するX 軸、Y 軸に加え、スペクトル横軸の次元をZ 軸にとった3 次元のハイパーキューブ・データを取り扱う。これらのデータセットから、互いに独立なスペクトル成分を多変量解析の手法によりモデルスペクトルとして抽出し、測定したポイントごとに各モデルスペクトルの寄与度を計算し、その寄与度の大きさを使ってイメージを作成する。ラマンバンドを選択する従来の方法と比較し、よりわずかなスペクトル差を識別して成分分布イメージを作成することができる。
5-4. 応用例:ガン細胞のラマンイメージング[4]
顕微ラマン分光装置を使って、タンパク質、多糖類、DNA/RNA、脂質をはじめ、生体内に蓄積された様々な化学物質を、単一細胞のレベルでイメージ化することができる。一例としてがん細胞ミエローマの測定例を紹介する。
ミエローマ細胞は、HeLa 細胞のような足場を持たず、ステージ移動操作に伴い容易に動く。そこで、試料ステージを固定しレーザ照射位置を走査して測定した。前述の多変量解析の手法により得られたラマンイメージを図5右に示す。左は顕微鏡観察イメージである。核成分が細胞内に多量に存在し、成分スペクトルのわずかな違いにより三種類の核酸(DNA)領域A、C、E に分類できている。
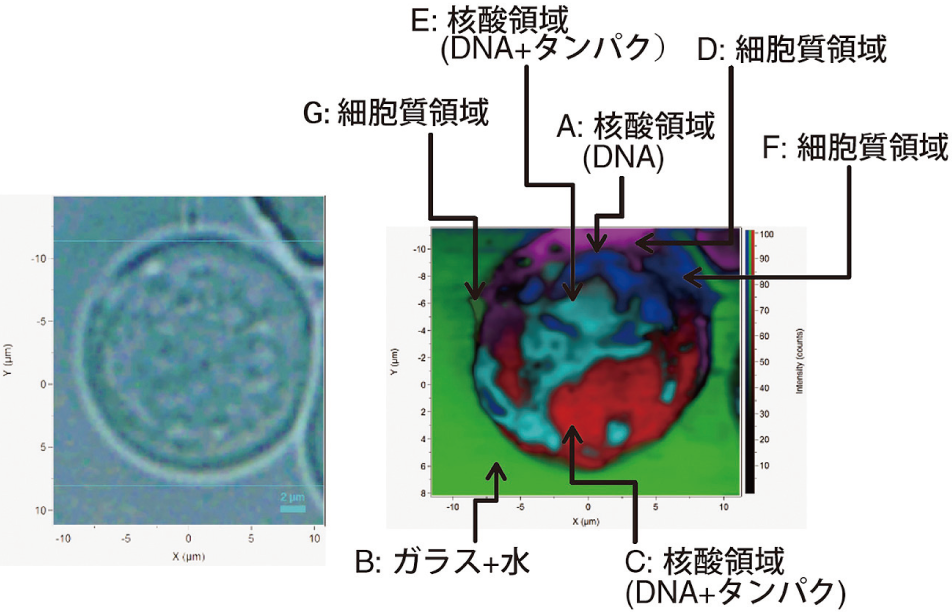
図5 ミエローマ細胞のラマンイメージ
- [1] 濱口宏夫, 岩田耕一, ラマン分光法(議談社, 2015).
- [2] J.Hirose, Readout, 40, 49(2013).
- [3] M. Komatsubara, T. Namazu, Y. Nagai, S. Inoue, N. Naka, S. Kashiwagi, K. Ohtsuki, Jph. J. Appl. phys., 48, 04C021(2009).
- [4] T. Numata et al. Readout , 45, 24(2015).
中田 靖
(株式会社堀場製作所)
2017年2月1日 公開












